Scandium, Sc, атомный номер 21
общий
Скандий (от латинского Scandia «Скандинавия») представляет собой химический элемент с символом Sc и атомным номером 21.
В периодической таблице это находится в 3. Подгруппа (группа 3) или скандиевая группа. Мягкий серебристо-белый элемент является первым из переходных металлов и также относится к металлам редкоземельных элементов.

Скандий металлический
Скандий был обнаружен 1879 Ларсом Фредриком Нильсоном. Из 10 кг эвксенита и гадолинита он выделил оксид с ранее неизвестными свойствами. Он назвал новый элемент, который он подозревал в честь своей родины, "Скандиум". Уже в 1869 Дмитрий Иванович Менделеев предсказал элемент Эка-Бор с атомным номером 21. Только Per Teodor Cleve позже узнал о согласии скандия с Eka-Boron.Pure Scandium 1937 был впервые получен электролитически из эвтектического расплава хлорида калия, лития и скандия при 700 до 800 ° C.
Скандий является одним из редких элементов. Элементаль это не происходит, только в некоторых редких минералах можно найти его в обогащенной форме:
Thortveitit: (Sc, Y) 2Si2O7
Эвксенит: (Y, Ca, Ce, U, Th) (Nb, Ta, Ti) 2O6
Gadolinit Y2Fe2+Be2Si2O10
Иксиолит: (Ta, Nb, Sn, Mn, Fe) 4O8
Bazzit: (Sc, Al) 2Be3Si6O18
Kolbeckite: ScPO4 · 2 H2O
Периодическая таблица скандий-21
Скандий обнаружен в низких концентрациях в минералах, превышающих 800. Поэтому он также включен в рудные концентраты переходных металлов как «примеси». К ним относятся российские и китайские вольфрамитовые и танталитовые концентраты. Соединения скандия также получают при переработке урансодержащих руд.
Синий цвет аквамарина, разновидности берилла, вызван ионами Sc3 +.
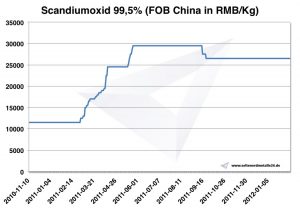
Диаграмма оксида скандия 2010-2012
восстановление
Исходным материалом в основном является тортвейт, который в несколько этапов перерабатывается в оксид скандия. Металлический скандий затем генерируется путем превращения во фтор и восстановления кальцием.
Особенности
Благодаря своей плотности скандий является одним из легких металлов. На воздухе становится тусклым, образует защитный слой желтоватого оксида. Скандий реагирует с разбавленными кислотами с образованием водорода и трехвалентных катионов. В водяном паре от 600 ° C реакция на Scandiumoxid Sc2O3. В водных растворах катионы Sc ведут себя подобно алюминию, что часто вызывает трудности при аналитическом разделении. Он должен быть стабильным в смеси азотной кислоты и 48% фтористого водорода.
Использовать
Его основное применение находит скандий в виде йодида скандия в высокоэффективных ртутных лампах высокого давления, например, для освещения стадионов. Вместе с гольмием и диспрозием создается свет, похожий на дневной. Скандий также используется для изготовления лазерных кристаллов. Магнитное хранилище данных оксида скандия добавляется для увеличения Ummagnetisierungsgeschwindigkeit. Скандий как хлорид скандия используется в микроколичествах как очень важный компонент в катализаторе при производстве хлористого водорода.
В качестве легирующей добавки скандий проявляет эффекты, стабилизирующие структуру и увеличивающие размер зерна. Алюминиево-литиевый сплав с низким добавлением скандия используется для изготовления некоторых компонентов в российских истребителях. Сплавы скандия также используются в современной велосипедной промышленности (см. Дорожный велосипед). Эти сплавы также содержат относительно мало скандия.
Порошок скандия является легковоспламеняющимся и поэтому классифицируется как легковоспламеняющийся.
| Общий | |
| Имя, символ
порядковый |
Скандий, Dc, 21 |
| серия | Переходные металлы |
| Группа, период, блок | 3, 4, д |
| Внешний вид | серебристо-белый |
| номер CAS | 7440-20-2 |
| Массовая доля земной оболочки | 5,1 частей на миллион |
| ядерной | |
| атомная масса | 44,955910 и |
| атомный радиус | 160 м. |
| Ковалентный радиус | 170 м. |
| Elektronenkonf. | [Ar] 3d (1) 4s2 |
| 1. ионизация | 633,1 кДж / моль |
| 2. ионизация | 1235,0 кДж / моль |
| 3. ионизация | 2388,6 кДж / моль |
| физически | |
| Физическое состояние | Праздник |
| кристаллическая структура | шестиугольный |
| плотность | 2,985 г / cm3 |
| магнетизм | парамагнитный (χm = 2,6 * 10 (-4)) |
| точка плавления | 1814 K (1541 C) |
| Температура кипения | 3103 K (2830 C) |
| Молярный объем | 15,00 * 10 (-6) м (3) / моль |
| Теплота парообразования | 318 кДж / моль |
| теплота плавления | 16,0 кДж / моль |
| Электропроводность | 1,81 * 10 (6) A / (V * m) |
| теплопроводность | 16 W / (м * К) |
