Самарий, Sm, атомный номер 62
общий
Самарий (в честь минерала Самарскит, который в свою очередь назван в честь горного инженера В.М. Самарского) - это химический элемент с символом Sm и атомным номером 62. В периодической таблице серебристый сияющий элемент относится к группе лантаноидов и, следовательно, также относится к металлам редкоземельных элементов.
Для открытия Самария в литературе есть несколько представлений.
1. 1853 продемонстрировал самарию швейцарского Жана Шарля Галиссара де Мариньяка спектроскопически с помощью четкой линии поглощения в дидимоксиде после. 1879 выделил французу Полю Эмилю Лекоку де Буабодрану элемент минерала Самарскит (Y, Ce, U, Fe) 3 (Nb, Ta, Ti) 5O16). Минеральное и элементное обозначение получено от российского горного инспектора полковника Самарского, который обнаружил минерал.
2. 1878 обнаружил швейцарского химика Марка Делафонтаина Самария, который он называет Decipum, в оксиде дидимия. 1879 независимо обнаруживает Самария Пола Эмиля Лекока де Буасбаудрана. 1881 показывает Делафонтену, что его изолированный элемент содержит еще один элемент, помимо самария.
3. Спектроскопическое открытие 1 Мариньяка, упомянутое в 1853, было сделано 1878 Полом Эмилем Лекоком де Буасбаудраном.
1903, немецкий химик Вильгельм Мутман, производил металлический самарий электролизом.
Конечно, элементарный самарий не встречается. Однако некоторые минералы, такие как монацит, бастназит и самарскит, содержат этот элемент. Монацит содержит до 1% самария.
восстановление
Начиная с монацита или бастнаезита, происходит разделение редкоземельных элементов посредством ионного обмена, экстракции растворителем или электрохимического осаждения. На заключительном этапе процесса высокочистый оксид самария с металлическим лантаном восстанавливают до металла и сублимируют.
Особенности
Самарий достаточно устойчив на воздухе, он образует пассивирующий желтоватый оксидный слой. Блестящий металлический самарий воспламеняется при температуре выше 150 ° C. Он реагирует с кислородом с образованием полуторного оксида Sm2O3. Он бурно реагирует с водой с образованием водорода и гидроксида самария. Как и у всех лантаноидов, наиболее стабильная степень окисления +3. Самарий выпускается в трех модификациях. Точки перехода - 734 ° C и 922 ° C. Катионы Sm3 + желтеют водные растворы.
Существует четыре стабильных и нестабильных радиоактивных изотопа 19. Наиболее распространенными природными изотопами являются 152Sm (26,7%), 154Sm (22,7%) и 147Sm (15%).
Использовать
Вместе с другими редкоземельными элементами для угольных дуговых ламп для пленочных проекционных систем.
Легирование монокристаллами фторида кальция для мазера и лазера.
Из-за своего большого теплового и эпитермального сечения нейтронов самарий используется в качестве поглотителя нейтронов в ядерных применениях.
Самарий Кобальт Магниты:
Постоянные магниты SmCo5 имеют высокое сопротивление размагничиванию и коэрцитивную силу до 2200 кА / м. Улучшенный сплав Sm2Co17 более дорог в производстве, но он обладает более высокими магнитными свойствами и повышенной коррозионной стойкостью.
Они используются в шаговых двигателях для кварцевых часов, приводных двигателях в миниатюрных ленточных устройствах (плееры, диктофоны), наушниках, датчиках, муфтах в мешалках и жестких дисках. В качестве энергосберегающих магнитных материалов они также используются в аэрокосмической промышленности.
Оксид самария добавляется в оптическое стекло для поглощения инфракрасного света.
Соединения самария используются для сенсибилизации (фосфора) фосфора при облучении инфракрасным светом.
В качестве катализатора; Оксид самария катализирует гидрирование и дегидрирование этанола (спирта).
В медицине изотоп 153Samarium используется в сочетании с бисфосфонатом (Lexidronam) для лечения болей в костях при раке (радионуклидная терапия метастазов в костях).
Соединения с самарием в менее благоприятной степени окисления + 2 (особенно йодид самария (II) и бромид самария (II)) находят применение в органическом синтезе (восстанавливающий агент и одноэлектронный реагент переноса, например, опосредованные самарием связи пинакола) ,
Совместно с радиофармацевтическим препаратом этилендиаминтетра (метиленфосфоновой кислоты) в ядерной медицине для паллиативного лечения костных и скелетных метастазов.
| Общий | |
| Имя, символ
порядковый |
Самарий, Sm, 62 |
| серия | лантаноиды |
| Группа, период, блок | La, 6, f |
| Внешний вид | серебристо-белый |
| номер CAS | 7440-19-9 |
| Массовая доля земной оболочки | 6 частей на миллион |
| ядерной | |
| атомная масса | 150,36 и |
| атомный радиус | 185 м. |
| Ковалентный радиус | 198 м. |
| Elektronenkonf. | [Xe] 4f (6) 6s2 |
| 1. ионизация | 544,5 кДж / моль |
| 2. ионизация | 1070 кДж / моль |
| 3. ионизация | 2260 кДж / моль |
| физически | |
| Физическое состояние | Праздник |
| кристаллическая структура | треугольный |
| плотность | 7,536 г / см3 (25 ° C) |
| магнетизм | парамагнитный (χm = 1,12 * 10 (-3)) |
| точка плавления | 1345 K (1072 C) |
| Температура кипения | 2076 K (1803 C) |
| Молярный объем | 19,98 * 10 (-6) м (3) / моль |
| Теплота парообразования | 175 кДж / моль |
| теплота плавления | 8,6 кДж / моль |
| Электропроводность | 1,06 * 10 (6) A / (V * m) |
| теплопроводность | 13 W / (м * К) |
Цены на самарий
Цены на самарий -> цены на редкоземельные элементы
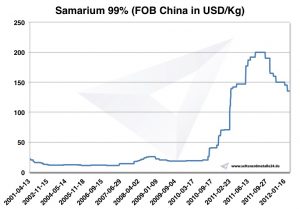
Диаграмма Самарий 2001-2012
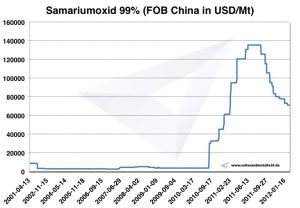
Диаграмма оксида самария 2001-2012