Сурьма, Sb, атомный номер 51
Сурьма цена, история, возникновение, добыча и использование
сурьма
Сурьма (от латинского Antimonium, вероятно, от арабского «al-ithmîd (un)») представляет собой химический элемент с символом элемента Sb (от латинского Stibium, (серый) щучий глянец) и атомным номером 51. В периодической таблице он указан в 5. Период и основная группа 5, или 15, группа IUPAC или группа азота. В стабильной модификации это серебристый и хрупкий полуметалл.
Имя, история
Также считается, что название восходит к позднегреческому гимну (немецкому цвету). Цель состояла в том, чтобы описать похожие на стебель кристаллы сульфида сурьмы, которые выглядели как пучки цветов и были похожи на цветок. В 11. Век находит себя латинским термином для антимониевого лекарственного препарата минеральной медицины для внутренней терапии болезней, а затем с Constantinus Africanus.
В 17. В 19 веке название сурьмы использовалось для обозначения металла. Коптский термин, обозначающий порошкообразный сульфид сурьмы, расшифровывается как греческий в латинском сурьме. Аббревиатура Sb, используемая шведским врачом и химиком Йенсом Якобом Берцелиусом («отец современной химии»), до сих пор используется как символ элемента.
Поздняя легендарная народная этимология, увековеченная Сэмюэлем Джонсоном в его словаре, говорит, что немецкий монах Василий Валентин заметил, что свиньи быстро толстеют, поглощая сурьму. Он также попробовал это на своих монахах, после чего они умерли, однако, так что был придуман термин «сурьма» (сурьма), из которого впоследствии была создана «сурьма».
Типичным местом для твердой сурьмы является серебряный рудник в шведском муниципалитете Сала в Вестманланде. Однако металлическая сурьма была уже известна китайцам и вавилонянам. Некоторые из его соединений уже использовались в бронзовом веке в качестве добавки к меди для производства бронзы (находки Велема Св. Вида в Венгрии).
Вхождение
Сурьма - редкий элемент. Так как он также может быть найден в природе (то есть в элементарной форме), он сертифицирован Международной минералогической ассоциацией (IMA) под номером системы. 1.CA.05 признан минералом.
Твердая сурьма (2011) была обнаружена во всем мире на сайтах 300. Так, в частности, в нескольких регионах Австралии; в боливийских департаментах Ла-Пас и Потоси; Минас-Жерайс в Бразилии; Шварцвальд, Фихтельгебирге, Верхний Пфальц, Оденвальд и Гарц в Германии; Сейняйоки в Финляндии; несколько регионов Франции; Ломбардия, Пьемонт, Сардиния и Трентино-Альто-Адидже в Италии; некоторые регионы Канады; некоторые регионы Австрии; Восточная и Западная Сибирь и Урал в России; кроме Вестманланда, Даларна, Гестрикленд, Нарке, Содерманланд, Вермланд и Вестерботтен в Швеции; в некоторых регионах Словакии; Богемия и Моравия в Чехии, а также во многих регионах США. Одним из наиболее важных в мире месторождений твердой сурьмы и руд сурьмы является зеленовато-коричневый пояс Мерчисон в пределах хребта Мерчисон в Южной Африке.
До настоящего времени известны минералы сурьмы 264 (по состоянию на 2010). В основном используется сульфидный минерал Stibnit Sb2S3 (Grauspießglanz) с максимальным содержанием 71,7% Sb. Минерал с самым высоким содержанием Sb в химическом соединении представляет собой природный сурьмяный мышьяковый сплав Paradocrasit (макс. 92%). Тем не менее, в отличие от Stibnit (вокруг сайтов 2500), он встречается только в трех местах, гораздо реже. Другими источниками сурьмы являются минералы Valentinit Sb2O3 (Weißspießglanz), Breithauptit NiSb (сурьма, никель, антимонид никеля), Kermesit Sb2S2O (красный блеск) и Sb2S5 (сера золота).
Извлечение и презентация
Технически сурьма извлекается из глянца сурьмы. Один метод основан на обжарке и восстановлении углеродом (восстановительный метод восстановления):
Другая возможность заключается в проведении восстановления железом (метод осаждения):
Во всем мире были в начале 21. Век между 110.000 и 160.000 тонн в год повышается сурьмы. Начиная с 1900, производительность увеличилась более чем в десять раз.
87% производства сурьмы осуществляется в Китае (по состоянию на 2015).
Свойства
Сурьма может встречаться в трех различных модификациях, причем наиболее последовательной является металлическая или серая сурьма.
При нормальных условиях сурьма кристаллизуется тригонально в ромбоэдрической установке в пространственной группе R3m (№ 166), описанной в соответствии с символикой Германа Могена с параметрами решетки a = 431 pm и c = 1127 pm, а также шесть формульных единиц на элементарную ячейку.
При охлаждении паров сурьмы на холодных поверхностях образуется аморфная, черная и высокореактивная сурьма, которая при нагревании превращается обратно в металлическую сурьму. При электролитическом производстве образуется взрывчатая сурьма, которая при растрескивании становится взрывно светящейся и искрится в металлическую сурьму. Однако эта форма всегда содержит некоторое количество хлора и не может рассматриваться как модификация. Желтая сурьма также является не самостоятельной модификацией, а высокополимерным химическим соединением с водородом.
Физические свойства
Металлическая сурьма серебристо-белая, очень блестящая, грубовато-кристаллическая. Это легко сокрушить из-за его хрупкости. Электрическая и теплопроводность низкая.
Химические свойства
С зарождающимся водородом сурьма реагирует с нестабильным гидридом сурьмы SbH3. Воздух и вода не атакуют сурьму при комнатной температуре. Выше точки плавления он горит на воздухе с голубовато-белым пламенем до оксида сурьмы (III). Растворяется в горячих концентрированных минеральных кислотах. С галогенами он активно реагирует при комнатной температуре на соответствующие галогениды.
В соединениях сурьма в основном присутствует в степени окисления + 3 и + 5. В антимонидах металлов, таких как антимонид калия K3Sb, он образует ионы Sb3.
Изотоп
Существует два стабильных изотопа сурьмы: 121Sb и 123Sb.
Использование и сплавы
Большая часть производимой сурьмы перерабатывается в сплавы и обладает следующими свойствами:
Служит для упрочнения сплавов свинца и олова. В отличие от большинства других металлов, он расширяется при охлаждении расплава (из-за превращения в другую модификацию): содержание сурьмы можно регулировать так, чтобы такие сплавы не давали усадки при усадке или даже несколько расширялись; Когда детали изготавливаются в литейных формах, металл прессуется во время затвердевания во всех углах и углах, так что даже сложные формы и поверхности с сильным рисунком можно сделать свободными от пустот.
Важные сплавы:
- Свинцово-сурьмянистые сплавы: твердый свинец, буквенный металл, несущий металл, свинцовый аккумулятор, свинцовая оболочка для подземных кабелей
- Сплавы олова и сурьмы: металл Британия, несущий металл
- Производство полупроводников, например. Б. легированием кремния для производства полупроводниковых соединений III V
- Сплавы олово-сурьма-медь (металл Баббит) для подшипниковых металлов
- Сплавы олово-сурьма-медь-свинец для оловянных и других изделий из олова
так называемый припой или мягкий припой - Алюминий сурьма, галлий сурьма, индий сурьма для инфракрасных устройств и устройств с эффектом Холла
- Безусадочные сплавы сурьмы для точного литья
Медицина
Сурьма (или препарат, полученный из руды сурьмы) была в 16. и 17. Стал (ятрохимическим) «ведущим лекарством», но, как и другие парацельсовые препараты, был спорным и также запрещенным во Франции между 1615 и 1688.
Камень зубного камня издавна использовался в качестве рефракционного агента (таблетки сурьмы), сегодня он до сих пор иногда используется для изучения содержимого желудка птиц.
И шистосомоз, и трипаносомы начинались в начале 19. Век с Брехвайнштейном (Калиумантимонилтартрат) сражался. Камень Тартар был изготовлен путем хранения вина в чашке сурьмы в течение одного дня, а затем пить его. Между тем используются более эффективные и более совместимые препараты.
Добавки сурьмы обычно используются в качестве менее токсичных пятивалентных форм для лекарственной терапии лейшманиоза и шистосомоза, но больше не являются препаратами первого выбора в развитых странах. Сурьма ингибирует фермент фосфофруктокиназу, которая является лимитирующей стадией гликолиза.
более
- Разжигание матча
- Часть взрывчатых веществ, детонаторов и свинцовых боеприпасов.
- Трисульфид сурьмы в тормозных накладках транспортных средств
Сурьма (V), сульфид: - для производства (вулканизации) красной резины (пример: шланги лабораторные резиновые)
- как красный компонент стреляющей головы в спичках
- раньше, чем макияж глаз и в офтальмологии («Augenerweiterer»)
- Хромат сурьмы как пигмент желтого цвета
оксиды сурьмы - Катализатор для производства полиэфира и ПЭТ (оксида сурьмы (III))
- в качестве белого пигмента для окрашивания полистирола, полиэтилена и полипропилена
- Производство белой глазури и фритты (фарфор)
- Очистка свинцового стекла
- легированный оловом в качестве прозрачно-проводящего покрытия (оксиды олова и сурьмы "ATO"), например, на стеклах, для изготовления дисплеев или в электропроводящих пигментах ("Minatec"), для напольных покрытий для рассеивания электростатических зарядов.
- в пигментах («Lazerflair») для лазерной маркировки пластиковых деталей, из-за сильного поглощения инфракрасного излучения обычным маркировочным лазером (Nd: YAG).
- в камуфляже из-за сильного инфракрасного поглощения.
- как огнезащитный состав и компонент огнестойких и огнестойких красок,
- Пластмасса и текстиль для оболочки кабелей, чехлы для автомобильных сидений, ткани для штор, детская одежда и многое другое. Ä.
- Соли сурьмы как компонент пестицидов, пятен и фейерверков
- Делитель для золота: для осаждения серебра из расплава золота
токсичность
Сурьма может быть смертельной при приеме внутрь от 200 до 1200 мг. В токсикологии известны три формы сурьмы, из которых газообразный гидрид сурьмы (Stiban, SbH3) является наиболее опасной формой, вызывающей массивный гемолиз. Вслед за токсичностью следует рвотное рвотное средство с трехвалентной («трехвалентной») сурьмой, тогда как пятивалентная сурьма является наименее токсичной.
Трехвалентная сурьма поглощается эритроцитами в течение первых двух часов после приема до 95% и, таким образом, обогащается главным образом в сильно перфузируемых органах. Выведение происходит главным образом за счет связывания с глютатионом через желчь с соответственно высокой энтерогепатической циркуляцией, и только небольшая часть выводится через почки. Антимонил тартрат калия выделяется до 90% в течение первого дня после приема пищи, остальное составляет 10% из-за более медленной кинетики элиминации в течение 16 дней.
Сурьма, как и мышьяк, как полагают, ингибирует функцию комплекса пируватдегидрогеназы, что приводит к дефициту внутриклеточного энергоносителя аденозинтрифосфата (АТФ). Это приводит к образованию хелатных комплексов между сурьмяной и тиольной группами соответствующих ферментов. В организме он токсичен для многих органов, включая пищеварительный тракт, печень, почки, сердце и центральную нервную систему. Наибольшая концентрация достигает сурьмы в печени, где она может перейти к гепатиту вплоть до печеночной недостаточности. В сердце происходят изменения ЭКГ с инверсией и уменьшением зубца Т и удлинением интервала QT. Острая почечная недостаточность может привести к временному или постоянному гемодиализу.
В дополнение к поддерживающим мерам, таким как инфузионная терапия (как для компенсации потери жидкости в результате рвоты, так и для защиты почек) и тщательного мониторинга показателей жизнедеятельности и ЭКГ, активированный уголь, N-ацетилцистеин в качестве предшественника глутатиона, используется для противомикробного отравления повышенная секреция и хелатирующий агент, например. Б. Димеркапрол.
Результаты исследований показывают, что соединения сурьмы раздражают кожу и слизистые оболочки. Эти соединения, вероятно, растворяются из пластика и текстиля.
Инструкции по технике безопасности и предельные значения
Из соединений сурьмы ЕС классифицирует фторид сурьмы как токсичный (T), а хлориды как едкие (C) и опасные для окружающей среды (N); все другие соединения сурьмы как вредные (Xn) и опасные для окружающей среды (N). Сама сурьма там не указана, согласно паспорту безопасности, она помечена как раздражающая.
Международное агентство по исследованию рака (IARC) классифицирует оксид сурьмы (III) как возможное канцерогенное вещество.
В ЕС питьевая вода имеет предел 5 мкг / л. При исследовании фруктовых соков, разлитых в ПЭТ-бутылки (для которых нет руководств), выявлены концентрации сурьмы до 44,7 мкг / л в концентратах соков в неразбавленном виде.
Сурьма была добавлена в 2016 ЕС в соответствии с Регламентом (ЕС) № 1907 / 2006 (REACH) в контексте оценки вещества в скользящем плане действий Сообщества (CoRAP). Он проведет переоценку воздействия вещества на здоровье человека или окружающую среду и, при необходимости, инициирует последующее наблюдение. Основными причинами поглощения сурьмы были опасения по поводу воздействия на работников, высокого (агрегированного) тоннажа, высокого коэффициента риска (RCR) и широкого использования, а также потенциального риска канцерогенных свойств. Переоценка проводится после 2018 и проводится Германией.
доказательство
предварительные испытания:
Окраска пламени: пламя бледно-синее, мало характерное. Phosphorsalzperle: бесцветный (нарушается всеми элементами, образующими цветной жемчуг)
Реакция обнаружения:
Восстановление базовыми металлами, например железом, цинком или оловом.
В некислотных растворах основные металлы восстанавливают катионы сурьмы Sb (III), Sb (V) и Sb (III) / (V) до металлической сурьмы:
2 Sb3 + + 3 Fe → 2 Sb + 3 Fe2 +
Вещество для проверки на сурьму помещают в раствор соляной кислоты и смешивают с железным порошком. В результате получается черный, слоистый осадок металлической сурьмы в растворе или непосредственно на железе. Доказательство железного гвоздя также возможно. Здесь черный налет на ногте является доказательством сурьмы, которая здесь откладывается элементарно.
Образец болота позволяет четко обнаружить сурьму. Когда пиролитически осажденное вещество (темное глянцевое зеркало) не растворяется в аммиачной перекиси водорода, мышьяк и германий исключаются в качестве возможных альтернатив.
Высокочувствительное определение крошечных следов сурьмы происходит с помощью гидридной техники атомной спектрометрии. В принципе, образец Марша связан с атомно-абсорбционной спектрометрией. Матричные эффекты раствора образца могут быть очень эффективно подавлены.
Другой метод заключается в обработке водного раствора, содержащего ионы сурьмы, раствором родамина В. Он образует цветной комплекс, который можно экстрагировать изопропиловым эфиром. Однако это свидетельство весьма неспецифично, поскольку ионы золота, кадмия, галлия, таллия, урана и вольфрама образуют окрашенные комплексы.
Связи
- Водород сурьмы, также называемый моностибан SbH3.
- Токсичный газ, который образуется из сурьмы и кислот.
- Дистибан (Sb2H4)
галогеновые соединения
- Фторид сурьмы (V) (SbF5) образует (согласно VSEPR) квадратную пирамиду и гибридизуется с sp3d
- Сурьма (V) хлорид (SbCl5)
- Сурьма (III) фторид (SbF3)
- Сурьма (III) хлорид (SbCl3)
- Сурьма (III) бромид (SbBr3)
- Сурьма (III) йодид (SbI3)
кислородные соединения
- Оксид сурьмы (III) (триоксид сурьмы, Sb2O3)
- Оксид сурьмы (III, V) (тетроксид сурьмы, Sb2O4)
- Оксид сурьмы (V) (пентаоксид сурьмы, Sb2O5)
- Сурьма кислота / тригидроксид сурьмы (H3SbO3 / Sb (OH) 3)
- Сурьма кислота / сурьма (III) кислота, SbOOH или HSbO2
- Антимоновая кислота (HSb (OH) 6)
соединения серы
- Трисульфид сурьмы, также называемый блеском сурьмы (Sb2S3)
Серо-черные блестящие металлические стебли. Исходный материал для производства металлической сурьмы. Растворим в сильных кислотах. Используйте для спичек, протирки очков и маскировочных красок (отражение ИК-света). - Пентасульфид сурьмы, ранее известный как сера золота (Sb2S5)
Другие соединения
- Фторид хлорида сурьмы (V) (SbCl4F) (катализатор для производства политетрафторэтилена («Тефлон»))
- Антимонид алюминия (AlSb)
- Антимонид галлия (GaSb)
- Индийский антимонид (InSb)
Диаграмма сурьмы 2005-2020
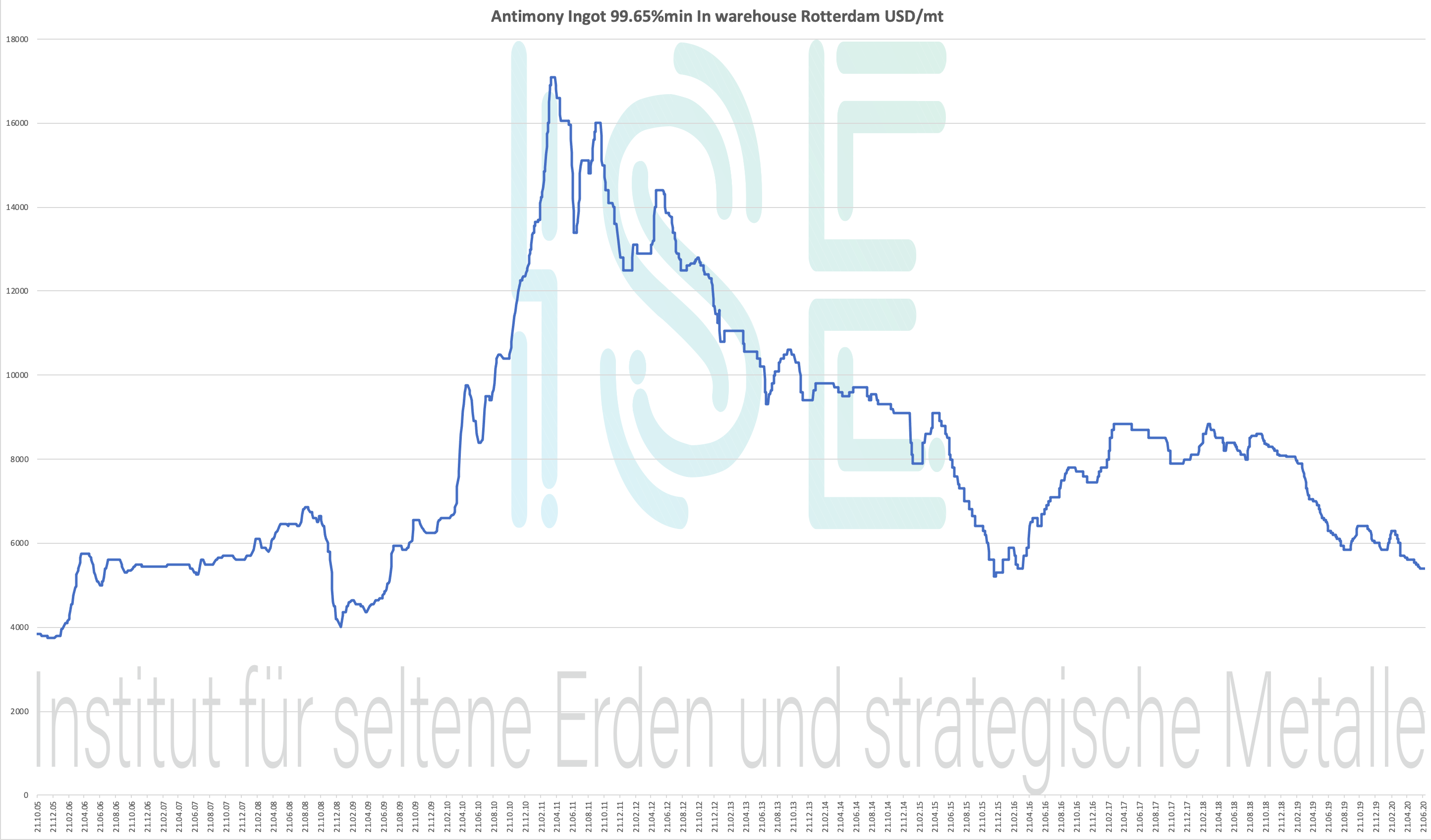
Слиток сурьмы 99.65% мин. На складе Роттердам USD / т
График цен 2004-2020 гг. - нажмите, чтобы увеличить
Цена сурьмы - ниже стратегической цены на металлы
Исторические данные о ценах на слиток сурьмы 99,65% склад Роттердам USD / т



