Тантал, Та, атомный номер 73
Цена, распространение, добыча и использование тантала
Тантал [ˈtantalum] - химический элемент с символом Ta и атомным номером 73; в периодической таблице он находится в пятой подгруппе или группе ванадия. Это редко встречающийся, пластичный, графитово-серый блестящий переходный металл. Тантал в основном используется для конденсаторов с большой емкостью и в то же время небольшого размера. Поскольку металл нетоксичен и инертен к биологическим жидкостям, он также используется для имплантатов, например, в качестве костного гвоздя.
Элемент был обнаружен в 1802 году Андерсом Густавом Экебергом в финской колумбитовой руде. Он отделил очень стабильный оксид (оксид тантала (V)), который не растворялся ни в какой кислоте. Он назван в честь Тантала, персонажа из греческой мифологии. По словам Экеберга, причина этого названия в том, что очень стойкий оксид «должен томиться и не может утолить свою жажду, как Тантал в подземном мире».
Почти в то же время Чарльз Хэтчетт обнаружил нечто очень похожее в колумбийской руде. ниобий. Эти два элемента считались идентичными до 1844 года, когда Генрих Роуз признал, что в колумбитовых рудах присутствуют два разных элемента, а именно тантал и колумбий. Он назвал последний ниобием.
После открытия нового элемента различные химики пытались представить тантал как элемент. Первым, кто произвел элементарный тантал путем восстановления фторида тантала калием, был Йенс Якоб Берцелиус в 1815 году. Однако, как и тантал, представленный Роуз, его металл на 50% состоит только из тантала. В 1902 году Анри Муассан попытался произвести тантал в электрической печи, но содержащийся в нем углерод сделал его продукт очень твердым и хрупким.
Первым, кто смог произвести чистый, пластичный тантал, был Вернер фон Болтон в 1903 году. Он добился этого, уменьшив количество раскаленных оксидов в вакууме и расплавив нечистый металлический тантал в вакууме и используя электрическую дугу пламени.
Первое применение нового элемента было в качестве нити накала в лампочках. Причина перехода с осмия, который ранее использовался, на тантал заключалась в том, что его легче обрабатывать, и он имеет более высокую возможную рабочую температуру до 2300 ° C. Позже он был заменен вольфрамом, который имеет еще более высокую температуру плавления и, таким образом, обеспечивает световой спектр, более близкий к солнечному, и более высокий световой поток.
В 1922 году тантал нашел новое применение в выпрямителях, а год спустя - в радиолампах.
Вхождение
Тантал - редкий элемент на Земле с содержанием 2 частей на миллион в континентальной коре и 8 частей на миллион в земной оболочке. Частота сопоставима с таковой мышьяка и германия. Внутри группы частота уменьшается в десять раз. Тантал не встречается в природе, а только в виде его соединений в различных минералах. Из-за схожести этих двух элементов танталовые руды всегда содержат ниобий и наоборот (социализация). Наиболее важными минералами являются минералы ряда колумбита и тапиолита, в которых различные минералы с общей формулой (Mn, Fe2+) (Nb, Та)2O6 Подводя итог. Коламбиты тантала также называют танталит назначен. Примерами минералов, содержащих тантал в этой серии, являются ферротапиолит (Fe2+, Мин2+) (Та, Nb)2O6 и марганцево-танталит MnTa2O6. Эти руды часто называют колтаном. Менее распространенные минералы - микролит или тореаулит.
Самыми крупными странами-производителями танталовых руд в 2007 году были Австралия - 850 тонн и Бразилия - 250 тонн. Колтан также встречается в Канаде и различных африканских странах, таких как Эфиопия, Мозамбик и Руанда. О месторождениях на востоке Демократической Республики Конго, которые яростно оспаривали во время войны в Конго 1996-2008 годов, стало известно в СМИ.
Извлечение и презентация
Поскольку тантал и ниобий всегда присутствуют вместе в рудах, используемых для извлечения тантала, их необходимо отделить для извлечения чистых металлов. Это осложняется большим сходством двух элементов.
Первый метод разделения был разработан Жаном Шарлем Галиссаром де Мариньяком в 1866 году. Он использовал различную растворимость двух элементов в разбавленной плавиковой кислоте. Тантал образует малорастворимый K2TaF7Ниобий хорошо растворимый К3NbOF5 · 2 H2O.
Технически используемый сегодня процесс основан на экстракции и использует различную растворимость сложных солей фтора в воде и некоторых органических растворителях. Рудную смесь сначала растворяют в концентрированной плавиковой кислоте или смесях плавиковой и серной кислот. Комплексные фториды [NbOF5]2- и [TaF7]2-. После того как нерастворимые компоненты отфильтрованы, разделение может быть проведено экстракцией жидкость-жидкость с помощью метилизобутилкетона. Если к раствору добавляют метилизобутилкетон, комплексы ниобия и тантала переходят в органическую фазу, в то время как другие элементы, такие как железо или марганец, остаются в водной фазе. При добавлении воды к отделенной органической фазе в ней растворяется только комплекс ниобия, тантал остается в метилизобутилкетоне.
С помощью фторида калия тантал можно превратить в малорастворимый калий.2[TaF7] быть срубленным. Восстановление до элементарного тантала в основном осуществляется натрием.
![\ mathrm {K_2 [TaF_7] + 5 \ Na \ longrightarrow Ta + 5 \ NaF + 2 \ KF}](https://upload.wikimedia.org/wikipedia/de/math/4/0/8/4082df7e6f3cde8acd65ddf4230284e5.png)
Восстановление натрием
Возможная альтернатива экстракции - фракционная перегонка. Для этой цели используются разные температуры кипения двух хлоридов пентахлорида ниобия и пентахлорида тантала. Их можно извлечь из руд с помощью хлора и кокса при высоких температурах. После разделения хлорид тантала также восстанавливается до металла натрием.
Помимо колумбит-танталитовых руд, шлак от плавки олова является важным источником для извлечения тантала (содержит несколько процентов тантала).
Физические свойства
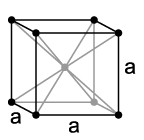
Кристаллическая структура тантала,a = 330,3 вечера
Тантал - это отчетливо пурпурно-серый, твердый как сталь (твердость по Виккерсу: 60–120 HV), тугоплавкий тяжелый металл, который по большинству своих свойств похож на ниобий. Он кристаллизуется в объемно-центрированной кубической кристаллической структуре. С температурой плавления около 3000 ° C тантал имеет самую высокую температуру плавления из всех элементов после вольфрама, углерода и рения. Если в металле хранится лишь небольшое количество углерода или водорода, температура плавления значительно увеличивается. Карбид тантала с температурой плавления 3880 ° C имеет одну из самых высоких температур плавления среди всех веществ.
Тантал становится сверхпроводником при температуре перехода ниже 4,3 Кельвина.
Хотя чистый тантал пластичен и может значительно растягиваться (предел прочности при растяжении: 240 МПа), даже небольшое количество углерода или водорода, добавленных к нему, значительно изменяет механическую прочность. Материал становится хрупким и трудно поддается обработке. Этот эффект используется для производства танталового порошка. В технологии в него добавляют водород и, таким образом, он охрупчивается, затем соответствующим образом измельчается и прокаливается или освобождается от водорода при более высокой температуре.
Химические свойства
Тантал является неблагородным металлом и при высоких температурах реагирует с большинством неметаллов, такими как кислород, галогены или углерод. Однако при комнатной температуре металл защищен тонким слоем оксида тантала (V) и, таким образом, пассивирован. Реакция протекает только при температуре около 300 ° C.
В большинстве кислот тантал не растворяется из-за пассивации, даже царская водка не может растворить металл. На тантал воздействуют только плавиковая кислота, олеум (смесь серной кислоты и триоксида серы) и расплавленные соли.
Изотоп
Всего имеется 30 изотопов и 26 ядерных изомеров 155Та вверх 185Та известен. Природный тантал состоит почти исключительно (99,988%) из изотопа 181Ta. Кроме того, основной изомер составляет 0,012% 180mТа раньше. Хотя теоретически он может быть радиоактивным, распада до сих пор не наблюдалось. Следовательно, период полураспада должен превышать 1 · 1015 быть лет.
Использовать
Большая часть тантала (мировой годовой объем производства 1.400 т) используется для изготовления очень маленьких конденсаторов с высокой емкостью. В 2007 году 60% тантала было использовано в производстве конденсаторов. Эти танталовые электролитические конденсаторы используются повсеместно в современной микроэлектронике, например, в сотовых телефонах и в автомобилестроении. Эффект основан на слое оксида тантала на поверхности намотанной танталовой фольги, которая остается стабильной и надежно изолирующей даже в очень тонкой версии. Чем тоньше слой между электродами, тем больше емкость при одинаковой поверхности фольги; Оксид тантала также имеет чрезвычайно высокую диэлектрическую проницаемость, что также увеличивает емкость.
Поскольку тантал нетоксичен и не вступает в реакцию с тканями или жидкостями организма, элементарный тантал используется для изготовления медицинских имплантатов и инструментов. Например, костные гвозди, протезы, зажимы и винты для челюстей изготавливаются из тантала. Кроме того, это рентгеноконтрастное вещество, которое мало используется из-за своей высокой стоимости.
В химической промышленности тантал используется из-за его прочности. Он служит облицовочным материалом для реакционных сосудов и используется для теплообменников и насосов. Для этих целей обычно используют не чистый тантал, а сплавы, содержащие 2,5–10% вольфрама. Они более стабильны и устойчивы, чем чистый тантал. При этом желаемая пластичность сохраняется. Другое применение - лабораторное оборудование, фильеры и катоды электронных ламп. Здесь тантал извлекает выгоду из того факта, что он способен поглощать до 800 частей по объему газа при 740 ° C (геттерный эффект), что обеспечивает высокий вакуум в трубках.
Суперсплавы, которые используются в конструкции турбин и авиационных двигателей, содержат до 9% тантала. Добавление 3–4% тантала в никелевый суперсплав увеличивает прочность материала при высоких температурах.
безопасности
Работа с танталом и его соединениями обычно не вызывает никаких проблем в лабораторных условиях. Элементарные соединения тантала и тантала не токсичны. Однако есть неопределенные указания на то, что некоторые соединения тантала являются канцерогенными. Танталовый порошок и пыль, как и другие мелкодисперсные металлы, представляют собой высокий риск возгорания и взрыва.
Связи
Оксид тантала (V) Ta2O5 это белый порошок, используемый для изготовления высоко преломляющих стекол и специальных кристаллических материалов.
Карбид тантала TaC с температурой плавления 3880 ° C и твердостью, близкой к алмазной, служит защитным слоем на жаропрочных сплавах двигателей и режущих инструментов.
| Общий | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Имя, символ, атомный номер | Тантал, Та, 73 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| серия | Переходные металлы | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Группа, период, блок | 5, 6, д | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешний вид | серый | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| номер CAS | 7440-25-7 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Массовая доля земной оболочки | 8 частей на миллион | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ядерной | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| атомная масса | 180,9479 XNUMX человека | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомный радиус (рассчитанный) | 145 (200) вечера | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ковалентный радиус | 138 м. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| электронная конфигурация | [Xe] 4f14 5d3 6s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. ионизация | 761 кДж / моль | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. ионизация | 1500 кДж / моль | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| физически | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Физическое состояние | Праздник | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| кристаллическая структура | кубическое тело-центрированное | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| плотность | 16,65 г / см3 (20 ° С) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| твердость по Моосу | 6,5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| магнетизм | парамагнитный ( = 1,8 10-4) = 1,8 10-4) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| точка плавления | 3290 К (3017 ° С) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Температура кипения | 5731 К (5458 ° С) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Молярный объем | 10,85 · 10-6 m3/ моль | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Теплота парообразования | 735 кДж / моль | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| теплота плавления | 36 кДж / моль | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| скорость звука | 3400 м / с на 293,15 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Удельная теплоемкость | 140 Дж / (кг · К) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Электропроводность | 7,61 · 106 А / (В · м) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| теплопроводность | 57 Вт / (м · К) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Химический | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| состояния окисления | 5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| нормальный потенциал | −0,81 В (½ Ta2O5 + 5 H.+ + 5 е- → Ta + 2½ H2O) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| электроотрицательность | 1,5 (шкала Полинга) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Изотоп | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| свойства ЯМР | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| безопасности | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Цены на тантал
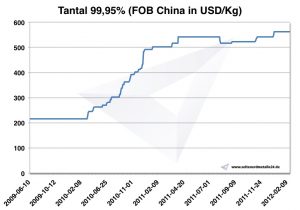
Диаграмма Тантал 2009-2012
Текущие цены на тантал


